REDOX*
Oxidación → Pérdida de electrones
Reducción → Ganancia de electrones
En una reacción óxido reducción siempre debe de haber un elemento que se oxida y uno que se reduce, para saberlo, es necesario calcular el No. de Oxidación de cada elemento de la reacción y compararlos para buscar a aquellos elementos que cambiaron su No. de oxidación.
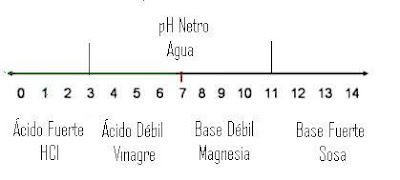
Posteriormente se usa la recta númerica que se encuentra a continuación para obtener todo lo necesario.
Cálculo de Valencia
Fe2O3
Primero se sacan las cargas (del lado izquierdo siempre es el catión (+) y del lado derecho siempre es el anión (-))
Fe+O-
Posteriormente se intercambian los átomos de cada elemento
Fe+3O-2
El 2 del Fe pasa a el O y el 3 del
O pasa al Fe
Entonces la valencia del Fe es +3 y del O-2
Ejemplo de REDOX
KClO3 → KCl + O2
K+1Cl+5O-2 → K+1Cl-1 + O 0
Cl +5 → Cl -1
O -2 → O 0
Siguiendo la recta numérica
El cloro se reduce y gana 6 electrones
El oxígeno se oxida y pierde 2 electrones
*Esto solo es una introducción a redox, para algo má detallado utiliza bibliografía especializada

Comentarios
Publicar un comentario